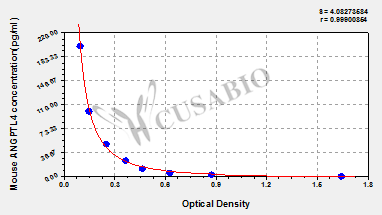
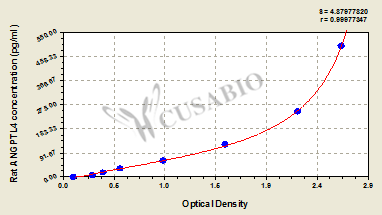
潛力新靶點ANGPTL4:連接代謝、炎癥與組織重塑的關鍵分子
日期:2026-02-04 17:15:07
血管生成素樣蛋白4(angiopoietin-like protein 4,ANGPTL4)是一種在多組織表達的分泌型糖蛋白,其生物學功能高度依賴組織來源、蛋白裂解狀態及病理背景。研究表明,ANGPTL4通過N端結構域抑制脂蛋白脂肪酶(lipoprotein lipase,LPL)活性,調控脂肪酸在不同組織間的分配,而其C端片段則主要參與細胞黏附、炎癥反應、血管通透性及組織重塑等非代謝過程。
近年來,大量證據顯示ANGPTL4在代謝性心血管疾病、腫瘤、腎臟疾病、神經退行性疾病及纖維化過程中發揮情境依賴性的雙重作用。本文系統梳理了ANGPTL4分子特征與核心信號通路,其在不同疾病中的作用機制、研究分歧及潛在轉化價值,并總結當前靶向ANGPTL4的藥物研發進展,為其作為生物標志物及治療靶點的臨床應用提供參考。
1. ANGPTL4的發現及基本生物學特征
ANGPTL4屬于ANGPTL家族成員,最初被鑒定為脂肪組織分泌的脂肪因子,隨后發現其在肝臟、腸道、肌肉、內皮細胞及多種腫瘤組織中均有表達。作為分泌蛋白,ANGPTL4可在胞外被蛋白水解為功能差異顯著的N端與C端片段,其表達與裂解受營養狀態、激素信號及炎癥環境調控。
在人類內臟脂肪組織中,ANGPTL4在伴隨葡萄糖代謝異常的肥胖個體中顯著上調,并與脂肪組織炎癥及脂肪細胞異質性相關,提示其可能參與代謝失衡的早期分子事件 [1]。體外研究顯示,ANGPTL4可通過形成復合體或裂解產物調節其對LPL的抑制效應,這一特性為其在不同生理和病理狀態下呈現差異化功能提供了分子基礎 [2]。臨床研究進一步將ANGPTL4與胰島素抵抗、血管功能障礙及炎癥狀態相關聯,奠定了其作為代謝—血管調節因子的研究基礎 [3,4]。
2. ANGPTL4的核心分子機制與信號通路
從機制上看,ANGPTL4最明確、證據最充分的作用靶點是LPL。遺傳學與功能研究一致表明,ANGPTL4通過抑制LPL活性限制富含甘油三酯脂蛋白的水解,從而調控脂肪酸進入脂肪組織、肌肉和肝臟的速率 [7,9]。這一作用在脂肪組織中尤為關鍵,其局部抑制或缺失可顯著改善全身脂質分配與胰島素敏感性 [7]。
除LPL外,ANGPTL4還通過與整合素、BMP/TGF-β信號組件及AKT/MTOR等通路發生互作,參與細胞存活、炎癥反應及組織重塑 [13,16]。這些通路并非在所有組織中同時激活,而是高度依賴細胞類型、蛋白片段形式及微環境因素,這種多層級調控構成了ANGPTL4功能異質性的分子基礎。
3. ANGPTL4在代謝性疾病與心血管疾病中的作用
在脂質代謝調控中,ANGPTL4通過抑制LPL改變組織對VLDL等富含甘油三酯脂蛋白的脂肪酸攝取,是調控血漿甘油三酯水平的重要因子。肝臟作為系統性脂質代謝樞紐,其分泌的ANGPTL4對外周脂蛋白代謝具有顯著影響。
肝靶向反義寡核苷酸(ASO)沉默Angptl4在APOE*3-Leiden.CETP小鼠中顯著降低血漿甘油三酯和膽固醇水平,并明顯縮小動脈粥樣硬化斑塊面積,同時在非人靈長類動物中表現出較好的短期耐受性,提示肝臟特異性干預在療效與安全性之間具備優勢 [19]。與此一致,肝細胞特異性Angptl4缺失模型通過增強肝脂蛋白酯酶活性,加速殘余脂蛋白清除,從而改善肥胖、胰島素抵抗和動脈粥樣化表型 [20]。
人群遺傳學證據進一步支持ANGPTL4在血脂調控中的因果作用。E40K等功能缺失變異與較低甘油三酯水平和更有利的代謝表型相關,并在肥胖人群中表現出一定的保護效應 [21]。然而,遺傳變異的終身效應與藥物干預的短期或中期作用并不完全等同,這一差異在解讀轉化潛力時需要謹慎權衡。
此外,ANGPTL4還被納入高血壓和代謝綜合征的分子網絡中。特定位點SNP與腰圍、血壓及代謝綜合征風險相關 [22],而高血壓患者中循環及脂肪組織ANGPTL4升高的觀察結果提示其可能參與血管張力調控和內皮功能改變 [23]。與此同時,腸道微生物通過調控腸道ANGPTL4表達影響脂質吸收和能量平衡,進一步凸顯了其在“肝—腸—外周組織”軸中的系統性作用 [24,25]。
4. ANGPTL4在腫瘤生物學中的雙重作用
ANGPTL4在腫瘤中的作用呈現高度情境依賴性,其既可作為促腫瘤因子,也可在特定背景下發揮抑癌效應。
在部分腫瘤模型中,ANGPTL4表現出抑癌特性。例如,在宮頸癌中,ANGPTL4過表達可抑制腫瘤細胞增殖、遷移和侵襲,并增強順鉑誘導的凋亡反應,而敲低則產生相反效應,提示其可能作為化療增敏因子。然而,這些結論主要基于體外模型,尚缺乏體內和臨床樣本層面的驗證。
在清晰細胞腎細胞癌中,ANGPTL4低表達與不良預后相關,其N端片段可通過抑制溶酶體酸性脂肪酶(LAL)限制脂質代謝驅動的腫瘤生長,提示ANGPTL4缺失狀態下腫瘤可能更依賴脂質代謝通路。
與上述抑癌效應相對,ANGPTL4在肥胖相關腫瘤微環境中常表現為促癌因子。在三陰性乳腺癌中,脂肪組織分泌因子通過PPARα-ANGPTL4軸重編程腫瘤脂質代謝,并通過FAK信號增強侵襲和遷移能力 [5]。此外,在肺腺癌中,ANGPTL4通過抑制焦亡和凋亡通路,促進EGFR抑制劑耐藥,揭示其在治療耐受形成中的潛在作用 [8]。
值得注意的是,ANGPTL4裂解片段在腫瘤中的功能存在顯著差異。研究表明,C端片段可促進腫瘤生長和轉移,而N端片段則抑制轉移并降低血管生成,這一現象強調蛋白加工狀態是決定其腫瘤學效應的關鍵變量。
5. ANGPTL4在腎臟、神經系統及纖維化疾病中的作用
在腎臟疾病中,ANGPTL4被證明參與脂質沉積、細胞衰老及纖維化進程。肥胖和衰老小鼠腎組織中ANGPTL4顯著上調,其過表達可促進腎小管上皮細胞脂質積累和衰老表型,而基因抑制則具有保護作用 [10]。在糖尿病腎病中,ANGPTL4通過與Integrin β1互作并激活STING通路,促進炎癥反應和上皮-間質轉化,從而加速腎間質纖維化 [11]。
在中樞神經系統,ANGPTL4被認為連接代謝異常與微膠質細胞功能失調。在阿爾茨海默病模型中,其上調與脂滴富集型微膠質細胞表型、氧化應激和炎癥增強密切相關,提示其可能介導肥胖與神經退行性疾病之間的病理聯系 [12]。
在血管生成和纖維化疾病中,ANGPTL4通過促進內皮-間質轉化(EndMT)參與脈絡膜新生血管和視網膜下纖維化形成,并可能影響抗VEGF治療反應 [17,18]。在肺纖維化模型中,ANGPTL4通過調控糖酵解重編程驅動間皮-間質轉化,提示其作為代謝-表型轉換節點的潛在價值 [6]。
6. 靶向ANGPTL4的藥物研發進展
ANGPTL4正成為代謝與炎癥相關疾病領域的一個新興藥物靶點。目前,圍繞該靶點已涌現出多種技術路線的在研藥物,涉及抗體、寡核苷酸及mRNA等不同類型,主要聚焦于脂代謝異常、心血管疾病及呼吸系統感染等適應癥。全球多家研發機構參與推進,部分項目已進入臨床中期試驗,整體研發進程活躍。部分研發管線整理如下表:
| 藥物 | 作用機制 | 藥物類型 | 在研適應癥 | 在研機構 | 最高研發階段 |
|---|---|---|---|---|---|
| MAR-001 | ANGPTL4抑制劑 | 單克隆抗體 | 高甘油三酯血癥 | 動脈粥樣硬化 | Marea Therapeutics Pty Ltd. | 臨床2期 |
| Lipisense | ANGPTL4抑制劑 | ASO | 高甘油三酯血癥 | 代謝綜合征 | 家族性乳糜微粒血癥綜合征 | Apotek Produktion & Laboratorier AB | Secarna Pharmaceuticals Gmbh & Co. | 成都先衍生物技術有限公司 | Lipigon Pharmaceuticals AB | 臨床2期 |
| CR-064 | ANGPTL4抑制劑 | Ang1抑制劑 | 單克隆抗體 | 腎細胞癌 | CuraGen Corp. | 臨床前 |
| ARDS treatment (Lipigon) | ANGPTL4抑制劑 | ASO | 急性呼吸窘迫綜合征 | Lipigon Pharmaceuticals AB | 臨床前 |
| P4 CAP (Lipigon Pharmaceuticals) | ANGPTL4抑制劑 | ASO | 社區獲得性肺炎 | Lipigon Pharmaceuticals AB | 臨床前 |
| WO2023044458 | - | 寡核苷酸 | 消化系統疾病 | 內分泌與代謝疾病 | 纖維化 | Alnylam Pharmaceuticals, Inc. | 藥物發現 |
| CN118853662 | - | mRNA | 心血管疾病 | 消化系統疾病 | 內分泌與代謝疾病 | 罕見病 | 成都先衍生物技術有限公司 | 藥物發現 |
(數據截止到2026年1月28日,來源于synapse)
7. ANGPTL4研究工具
ANGPTL4是連接脂質代謝、炎癥反應與組織重塑的關鍵分子,其生物學效應高度依賴組織來源、蛋白片段形式及病理背景。盡管現有研究已揭示其在多系統疾病中的重要作用,但功能異質性和物種差異仍是臨床轉化的主要挑戰。華美生物提供ANGPTL4重組蛋白、抗體、ELISA檢測試劑盒相關產品,助力您的基礎科研或藥物開發:
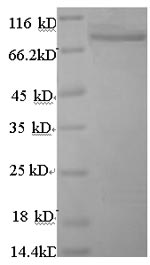
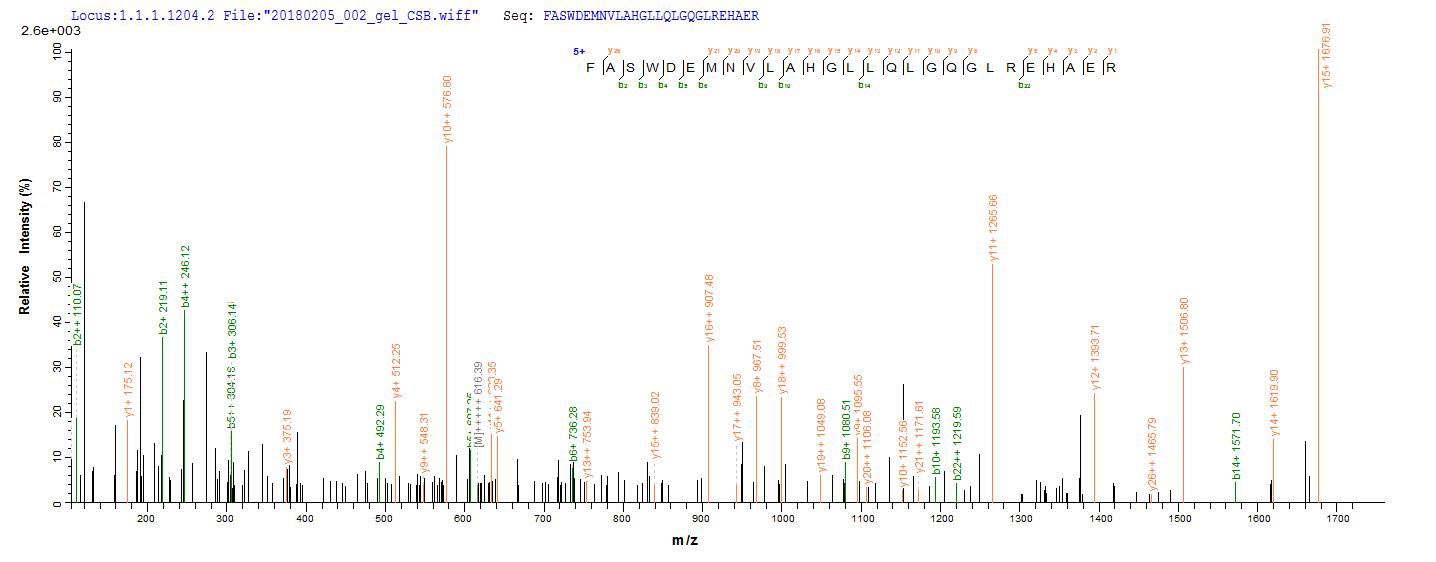
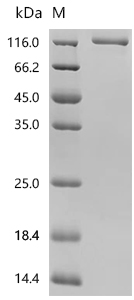
● ANGPTL4重組蛋白
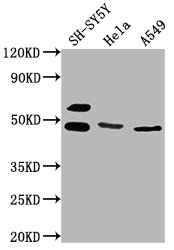
● ANGPTL4抗體
ANGPTL4 Antibody; CSB-PA866314ESR2HU
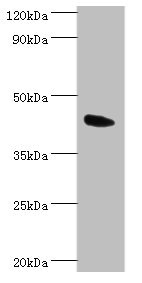
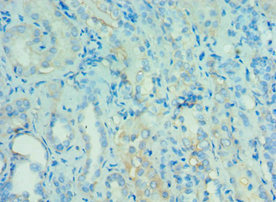
ANGPTL4 (MAR-001 Biosimilar) Recombinant Monoclonal Antibody
CSB-RA866314MB1HU
● ANGPTL4 ELISA試劑盒
[1] Ilaria Barchetta, Caterina Chiappetta, Valentina Ceccarelli, Flavia Agata Cimini, Laura Bertoccini, Melania Gaggini, Claudio Di Cristofano, Gianfran?o Silecchia, Andrea Lenzi, Frida Leonetti, Marco Giorgio Baroni, Amalia Gastaldelli, Maria Gisella Cavallo.(2020). Angiopoietin-Like Protein 4 Overexpression in Visceral Adipose Tissue from Obese Subjects with Impaired Glucose Metabolism and Relationship with Lipoprotein Lipase.
[2] Günther Silbernagel, Yan Q Chen, Hongxia Li, Deven Lemen, Yi Wen, Eugene Y Zhen, Martin Rief, Marcus E Kleber, Graciela E Delgado, Mark A Sarzynski, Yue-Wei Qian, Boerge Schmidt, Raimund Erbel, Ulrike S Trampisch, Angela P Moissl, Henrik Rudolf, Heribert Schunkert, Andreas Stang, Winfried M?rz, Hans J Trampisch, Hubert Scharnagl, Robert J Konrad.(2025). Associations of Circulating ANGPTL3, C-Terminal Domain-Containing ANGPTL4, and ANGPTL3/8 and ANGPTL4/8 Complexes with LPL Activity, Diabetes, Inflammation, and Cardiovascular Mortality.
[3] Haohua Wang, Wanying Luo, Min Lin, Xiaojing Li, Guangda Xiang, Silvia d Triganti.(2021). Plasma asprosin, CCDC80 and ANGPTL4 levels are associated with metabolic and cardiovascular risk in patients with inflammatory bowel disease.
[4] Francesca Schinzari, Giuseppina Vizioli, Umberto Campia, Manfredi Tesauro, Carmine Cardillo.(2021). Variable Changes of Circulating ANGPTL3 and ANGPTL4 in Different Obese Phenotypes: Relationship with Vasodilator Dysfunction.
[5] Christina Blücher, Sabine Iberl, Nancy Schwagarus, Silvana Müller, Gerhard Liebisch, Marcus H?ring, Maria Soledad Hidrobo, Josef Ecker, Nick Spindler, Arne Dietrich, Ralph Burkhardt, Sonja C. Stadler.(2020). Secreted Factors from Adipose Tissue Reprogram Tumor Lipid Metabolism and Induce Motility by Modulating PPARα/ANGPTL4 and FAK.
[6] Yuechong Xia, Fang Zhou, Hongyan Hui, Liping Dai, Songyun Ouyang.(2024). ANGPTL4 mediated mesothelial-mesenchymal transition in pulmonary fibrosis: a potential therapeutic target.
[7] Binod Aryal, Abhishek K. Singh, Xinbo Zhang, Luis Varela, Noemí Rotllán, Leigh Goedeke, Balkrishna Chaube, Jo?o Paulo Camporez, Daniel F. Vatner, Tamas L. Horváth, Gerald I. Shulman, Yajaira Suárez, Carlos Fernández‐Hernando.(2018). Absence of ANGPTL4 in adipose tissue improves glucose tolerance and attenuates atherogenesis.
[8] Yue Fang, Xuan Li, Hao Cheng, Lu Zhang, Jiqing Hao.(2022). ANGPTL4 Regulates Lung Adenocarcinoma Pyroptosis and Apoptosis via NLRP3\ASC\Caspase 8 Signaling Pathway to Promote Resistance to Gefitinib.
[9] Fredrik Landfors, Elin Chorell, Sander Kersten.(2022). Genetic Mimicry Analysis Reveals the Specific Lipases Targeted by the ANGPTL3-ANGPTL8 Complex and ANGPTL4.
[10] Xiaojun Wang, Hung-Chen Chang, Xuchao Gu, Wanlin Han, Shihang Mao, Lili Lu, Shuai Jiang, Haiyong Ding, Shisheng Han, Xinkai Qu, Zhijun Bao.(2024). Renal lipid accumulation and aging linked to tubular cells injury via ANGPTL4.
[11] Swayam Prakash Srivastava, Han Zhou, Rachel Shenoi, Myshal Morris, Bego?a Lainez, Leigh Goedeke, Barani Kumar Rajendran, Ocean Setia, Binod Aryal, Keizo Kanasaki, Daisuke Koya, Ken Inoki, Alan Dardik, Thomas Bell, Carlos Fernández‐Hernando, Gerald I. Shulman, Julie E. Goodwin.(2024). Renal Angptl4 is a key fibrogenic molecule in progressive diabetic kidney disease.
[12] Nan Li, Xiaojun Wang, Ruilang Lin, Fuxia Yang, Hung-Chen Chang, Xuchao Gu, Jun Shu, Guidong Liu, Yongfu Yu, Wenshi Wei, Zhijun Bao.(2024). ANGPTL4-mediated microglial lipid droplet accumulation: Bridging Alzheimer's disease and obesity.
[13] Yun Bai, Guanghua Cui, Xiaoke Sun, Meiqi Wei, Yanying Liu, Jialu Guo, Yu Yang.(2024). ANGPTL4 Stabilizes Bone Morphogenetic Protein 7 Through Deubiquitination and Promotes HCC Proliferation via the SMAD/MAPK Pathway.
[14] Xiujin Shen, Haibing Wang, Chunhua Weng, Yongchun He, Xue Shao, Jingyun Le, Hui Chen, Qixia Shen, Jianghua Chen, Hong Jiang.(2025). Angiopoietin-like 4 exacerbates renal tubular epithelial cell pyroptosis in acute kidney injury via integrin β5/FAK signaling pathway.
[15] Tin May Aung, Atit Silsirivanit, Apinya Jusakul, Waraporn Chan-On, Tanakorn Proungvitaya, Sittiruk Roytrakul, Siriporn Proungvitaya.(2022). Prediction of Angiopoietin-like Protein 4-related Signaling Pathways in Cholangiocarcinoma Cells.
[16] Xiao Song, Wang Nai‐dong, Jinxiang Yan, Long Tian, Xiurong Lu, Gao Hong, Yan Jie‐Cheng, Zhang Fei.(2022). ANGPTL4 regulate glutamine metabolism and fatty acid oxidation in nonsmall cell lung cancer cells.
[17] Jia Chen, Ying Yang, Shu Su, Shenglai Zhang, Ju Huang, Hong Chen, Xiaowei Yang, Aimin Sang.(2024). ANGPTL4 promotes choroidal neovascularization and subretinal fibrosis through the endothelial?mesenchymal transition.
[18] Deepti Sharma, Evan Lau, Yu Qin, Kathleen Jee, Murilo Rodrigues, Chuanyu Guo, Aumreetam Dinabandhu, Emma McIntyre, Shaima Salman, Yousang Hwang, Ala Moshiri, Gregg L Semenza, Silvia Montaner, Akrit Sodhi.(2024). VEGF inhibition increases expression of HIF-regulated angiogenic genes by the RPE limiting the response of wet AMD eyes to aflibercept.
[19] Melanie Modder, Wietse In Het Panhuis, Mohan Li, Salwa Afkir, Alexandra L Dorn, Amanda C M Pronk, Trea C M Streefland, Reshma A Lalai, Stefan Pierrou, Stefan K Nilsson, Gunilla Olivecrona, Sander Kooijman, Patrick C N Rensen, Milena Sch?nke.(2024). Liver-targeted Angptl4 silencing by antisense oligonucleotide treatment attenuates hyperlipidaemia and atherosclerosis development in APOE*3-Leiden.CETP mice.
[20] Abhishek K. Singh, Balkrishna Chaube, Xinbo Zhang, Jonathan Sun, Kathryn M. Citrin, Alberto Canfrán‐Duque, Binod Aryal, Noemí Rotllán, Luis Varela, Richard Lee, Tamas L. Horváth, Nathan L. Price, Yajaira Suárez, Carlos Fernández‐Hernando.(2021). Hepatocyte-specific suppression of ANGPTL4 improves obesity-associated diabetes and mitigates atherosclerosis in mice.
[21] Diego Bailetti, Laura Bertoccini, Rosellina Margherita Mancina, Ilaria Barchetta, Danila Capoccia, Efisio Cossu, Arturo Pujia, Andrea Lenzi, Frida Leonetti, Maria Gisella Cavallo, Stefano Romeo, Marco Giorgio Baroni.(2018). ANGPTL4 gene E40K variation protects against obesity‐associated dyslipidemia in participants with obesity.
[22] Zhoujie Tong, Jie Peng, Hongtao Lan, Wenwen Sai, Yulin Li, Jiaying Xie, Yanmin Tan, Wei Zhang, Ming Zhong, Zhihao Wang.(2021). Cross-talk between ANGPTL4 gene SNP Rs1044250 and weight management is a risk factor of metabolic syndrome.
[23] Mohamed Abu‐Farha, Preethi Cherian, Mohamed G. Qaddoumi, Irina Al‐Khairi, Sriraman Devarajan, Muath Alanbaei, Jehad Abubaker.(2018). Increased plasma and adipose tissue levels of ANGPTL8/Betatrophin and ANGPTL4 in people with hypertension.
[24] Jing Guo, Mengyuan Zhang, He Wang, Na Li, Zongliang Lu, Long Li, Suocheng Hui, Hongxia Xu.(2022). Gut microbiota and short chain fatty acids partially mediate the beneficial effects of inulin on metabolic disorders in obeseob/obmice.
[25] Sang‐Hyun Cho, Yong‐Joon Cho, Joo‐Hong Park.(2021). The human symbiont Bacteroides thetaiotaomicron promotes diet-induced obesity by regulating host lipid metabolism.