CRLF2(TSLPR): 連接2型炎癥與血液腫瘤的關(guān)鍵靶點(diǎn)
日期:2025-12-08 13:09:16
胸腺基質(zhì)淋巴細(xì)胞生成素受體(TSLPR,又稱CRLF2)是介導(dǎo)上皮源性細(xì)胞因子TSLP信號(hào)傳導(dǎo)的關(guān)鍵受體亞單位,與IL-7Rα共同構(gòu)成功能性受體復(fù)合物。TSLP/TSLPR通路在調(diào)控2型炎癥反應(yīng)中處于上游樞紐位置,不僅參與哮喘、慢性鼻竇炎伴鼻息肉(CRSwNP)和慢性阻塞性肺疾病(COPD)等免疫介導(dǎo)性疾病的發(fā)病機(jī)制,還在Ph樣急性淋巴細(xì)胞白血病等血液腫瘤中因異常激活而驅(qū)動(dòng)疾病進(jìn)展。
近年來,隨著對(duì)TSLPR生物學(xué)功能的深入理解,該靶點(diǎn)逐漸成為連接炎癥與腫瘤治療的重要橋梁。其中,全球目前唯一處于臨床開發(fā)階段的TSLP受體拮抗劑Verekitug(UPB-101),在2025年取得了關(guān)鍵性突破,進(jìn)一步凸顯了該靶點(diǎn)在慢性氣道炎癥性疾病中的治療潛力。
1. CRLF2的結(jié)構(gòu)和功能基礎(chǔ)
CRLF2(cytokine receptor-like factor 2),又稱胸腺基質(zhì)淋巴細(xì)胞生成素受體(TSLPR),是I型細(xì)胞因子受體超家族成員,編碼該蛋白的基因位于X和Y染色體的假常染色體1區(qū)(PAR1)。CRLF2本身不具激酶活性,需與白介素-7受體α鏈(IL-7Rα)形成異源二聚體,共同構(gòu)成胸腺基質(zhì)淋巴細(xì)胞生成素(TSLP)的功能性高親和力受體復(fù)合物 [1]。
1.1 蛋白結(jié)構(gòu)域組成
CRLF2為I型跨膜糖蛋白,由約370個(gè)氨基酸組成,包含一個(gè)N端胞外結(jié)構(gòu)域、一個(gè)單次跨膜區(qū)和一個(gè)C端短胞內(nèi)尾部。其胞外區(qū)含有I型細(xì)胞因子受體家族標(biāo)志性WSXWS基序,對(duì)維持受體構(gòu)象及配體結(jié)合至關(guān)重要。然而,與典型I型受體相比,CRLF2結(jié)構(gòu)具有明顯非典型性:其胞外結(jié)構(gòu)域缺失四個(gè)保守半胱氨酸殘基中的第二個(gè),可能影響二硫鍵形成與整體折疊;胞內(nèi)區(qū)雖保留Box1基序(用于JAK激酶錨定),卻缺乏經(jīng)典的Box2結(jié)構(gòu)域;此外,其胞內(nèi)尾部?jī)H含一個(gè)酪氨酸殘基,位于羧基末端上游第4位,且該位點(diǎn)在配體結(jié)合后并不發(fā)生磷酸化。這些特征表明,CRLF2自身無法獨(dú)立完成完整的信號(hào)轉(zhuǎn)導(dǎo),必須依賴共受體提供功能補(bǔ)償。
1.2 受體復(fù)合物組裝與配體識(shí)別
CRLF2自身無法獨(dú)立傳導(dǎo)信號(hào),必須與IL-7Rα共表達(dá)并形成異源二聚體,方能高親和力結(jié)合TSLP。TSLP首先與CRLF2的D1結(jié)構(gòu)域結(jié)合,誘導(dǎo)構(gòu)象變化后招募IL-7Rα,最終形成穩(wěn)定的三元復(fù)合物。這一組裝機(jī)制不僅實(shí)現(xiàn)了高親和力配體識(shí)別,還確保了信號(hào)激活的時(shí)空精確性,避免非特異性免疫激活。
2. CRLF2的相關(guān)信號(hào)通路
2.1 非經(jīng)典的JAK-STAT激活機(jī)制
TSLP結(jié)合CRLF2/IL-7Rα復(fù)合物后,可誘導(dǎo)下游信號(hào)級(jí)聯(lián)。傳統(tǒng)觀點(diǎn)認(rèn)為該過程涉及JAK1(結(jié)合IL-7Rα)與JAK2(結(jié)合CRLF2)的反式磷酸化,進(jìn)而激活STAT5。然而,深入研究表明,TSLP誘導(dǎo)的STAT5活化并不依賴典型的JAK激酶活性——顯性負(fù)性JAK1或JAK2無法阻斷該過程,而Tec家族激酶的抑制則可部分削弱STAT5磷酸化,提示Tec激酶可能在該通路中發(fā)揮關(guān)鍵作用。此外,STAT5的激活與其驅(qū)動(dòng)的細(xì)胞增殖功能并非線性耦合:STAT5活化不依賴CRLF2胞內(nèi)唯一的酪氨酸殘基,而該位點(diǎn)對(duì)細(xì)胞增殖卻至關(guān)重要。
2.2 多通路協(xié)同調(diào)控細(xì)胞命運(yùn)
除STAT5外,TSLP/CRLF2信號(hào)還可激活多條平行通路。Src家族激酶參與調(diào)控細(xì)胞增殖,其抑制劑可顯著阻斷TSLP誘導(dǎo)的增殖反應(yīng),但不影響STAT5磷酸化。同時(shí),該通路亦可激活MAPK/ERK和PI3K/AKT/mTOR通路,分別調(diào)控細(xì)胞周期進(jìn)程與抗凋亡程序。在病理狀態(tài)下,如Ph-like急性淋巴細(xì)胞白血病中,CRLF2的異常表達(dá)或突變可導(dǎo)致這些通路持續(xù)活化,共同驅(qū)動(dòng)白血病克隆的擴(kuò)增與存活。
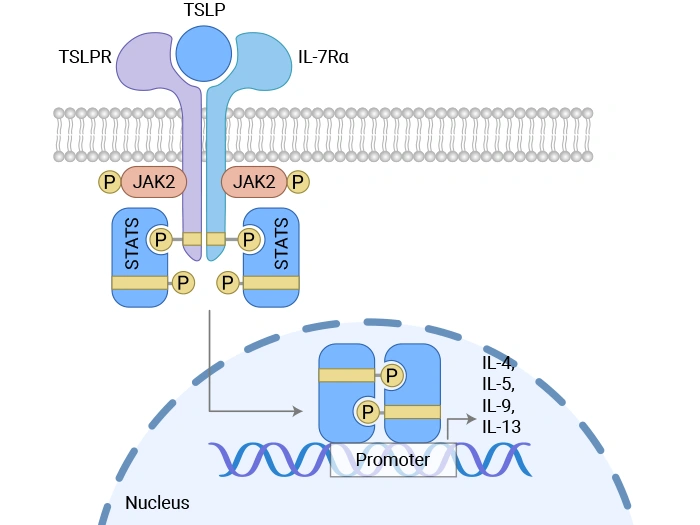
圖. 胸腺基質(zhì)淋巴細(xì)胞生成素誘導(dǎo)信號(hào)傳導(dǎo)的機(jī)制 [2]
3. CRLF2與疾病
● CRLF2與Ph樣急性淋巴細(xì)胞白血病
CRLF2異常是費(fèi)城染色體樣急性淋巴細(xì)胞白血病(Philadelphia chromosome–like acute lymphoblastic leukemia, Ph-like ALL)中最常見且最具臨床意義的分子特征之一。Ph-like ALL 是一種高危B細(xì)胞前體急性淋巴細(xì)胞白血病(BCP-ALL)亞型,其基因表達(dá)譜與費(fèi)城染色體陽(yáng)性(Ph+)ALL相似,但缺乏BCR-ABL1融合基因,取而代之的是多種激酶通路激活的遺傳改變,其中CRLF2重排或過表達(dá)占比最高 [3]。臨床上,CRLF2高表達(dá)與初診高白細(xì)胞計(jì)數(shù)、誘導(dǎo)治療后微小殘留病(MRD)清除不佳、復(fù)發(fā)風(fēng)險(xiǎn)升高及生存率下降顯著相關(guān) [4]。目前,CRLF2已被納入國(guó)際ALL診療指南作為Ph-like ALL的核心診斷標(biāo)志,并成為靶向治療的重要突破口
● CRLF2與哮喘
在哮喘,尤其是重度嗜酸性或Th2高型哮喘中,氣道上皮細(xì)胞因環(huán)境刺激(如過敏原、病毒、污染物)損傷而大量分泌TSLP。TSLP通過結(jié)合樹突狀細(xì)胞、2型固有淋巴細(xì)胞(ILC2s)和Th2細(xì)胞表面的CRLF2/IL-7Rα復(fù)合物,激活STAT5/STAT3通路,促進(jìn)IL-4、IL-5、IL-13等2型細(xì)胞因子釋放,驅(qū)動(dòng)嗜酸性粒細(xì)胞浸潤(rùn)、氣道高反應(yīng)性和黏液高分泌。臨床研究顯示,哮喘患者支氣管活檢組織和血清中TSLP及CRLF2表達(dá)水平顯著升高,且與疾病嚴(yán)重程度正相關(guān) [5]。
● CRLF2與過敏
TSLP作為過敏性炎癥級(jí)聯(lián)反應(yīng)的上游關(guān)鍵因子,通過其受體TSLPR(CRLF2)激活樹突狀細(xì)胞、Th2細(xì)胞和ILC2,驅(qū)動(dòng)2型免疫應(yīng)答;研究顯示,新型抗TSLPR全人源單克隆抗體ASP7266可有效阻斷TSLP信號(hào)傳導(dǎo),抑制TSLP誘導(dǎo)的細(xì)胞增殖、趨化因子CCL17釋放、Th2分化及ILC2來源的IL-5產(chǎn)生,并在食蟹猴模型中完全抑制過敏性皮膚反應(yīng),展現(xiàn)出優(yōu)于或媲美tezepelumab的臨床前藥理活性,有望成為哮喘、慢性鼻竇炎伴鼻息肉和特應(yīng)性皮炎等過敏性疾病的新一代靶向治療選擇 [6]。
4. CRLF2靶向藥物研究進(jìn)展
當(dāng)前針對(duì)TSLPR(即CRLF2)靶點(diǎn)的在研藥物涵蓋多種藥物類型,包括單克隆抗體、抗體偶聯(lián)藥物(ADC)和雙特異性抗體(BsAb)。在過敏炎癥性疾病領(lǐng)域,以阻斷配體-受體相互作用為核心的單克隆抗體(如處于臨床2期的Verekitug)進(jìn)展較快;而在血液腫瘤(尤其是Ph樣急性淋巴細(xì)胞白血病)領(lǐng)域,研發(fā)聚焦于通過抗體偶聯(lián)藥物和雙特異性抗體等新型技術(shù)實(shí)現(xiàn)靶向細(xì)胞殺傷,但目前多項(xiàng)在研項(xiàng)目尚處于臨床前探索階段,整體轉(zhuǎn)化進(jìn)程仍屬早期。
| 藥物 | 靶點(diǎn) | 藥物類型 | 在研適應(yīng)癥 | 在研機(jī)構(gòu) | 最高研發(fā)階段 |
|---|---|---|---|---|---|
| Verekitug | TSLPR | 單克隆抗體 | 慢性阻塞性肺疾病、重度哮喘、慢性鼻竇炎伴鼻息肉 | Upstream Bio, Inc. | 臨床2期 |
| AM E3-SG3249 | TSLPR | ADC | Ph樣急性淋巴細(xì)胞白血病 | IRBM SpA | 臨床前 |
| CRLF2-DM1 | TSLPR x Tubulin | ADC | Ph樣急性淋巴細(xì)胞白血病 | The University of New South Wales | 臨床前 |
| 1B7/CD3 BsAb(MD Anderson) | CD3 x TSLPR | 雙特異性抗體 | 急性淋巴細(xì)胞白血病 | The University of Texas MD Anderson Cancer Center | 臨床前 |
| Anti TSLP antibody | TSLPR | 單克隆抗體 | 自身免疫性疾病 | 華潤(rùn)生物醫(yī)藥有限公司 | 臨床前 |
(數(shù)據(jù)截止到2025年11月20日,來源于synapse)
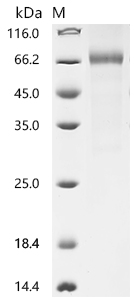
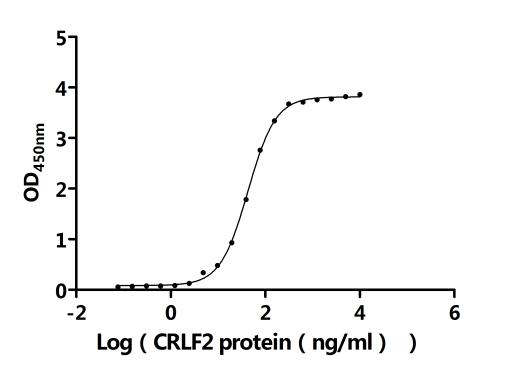
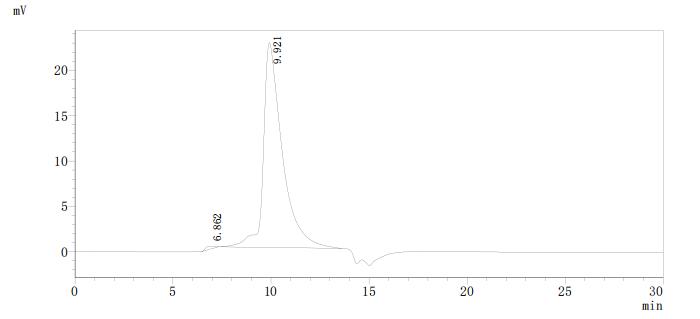
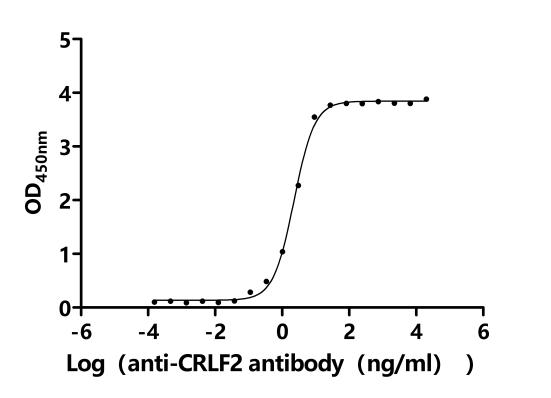
5. CRLF2研究工具
參考文獻(xiàn):
[1] Liu Y J, Soumelis V, Watanabe N, et al. TSLP: an epithelial cell cytokine that regulates T cell differentiation by conditioning dendritic cell maturation. Annu Rev Immunol. 2007; 25: 193-219.
[2] Ebina-Shibuya R,Leonard W J. Role of thymic stromal lymphopoietin in allergy and beyond. Nat Rev Immunol. 2023;23 (1):24-37.
[3] Potter N, Jones L, Blair H, et al. Single-cell analysis identifies CRLF2 rearrangements as both early and late events in Down syndrome and non-Down syndrome acute lymphoblastic leukaemia. Leukemia. 2019;33 (4):893-904.
[4] Jiang M, Zou X, Lu L. Potential efficacy and prognosis of silencing the CRLF2?mediated AKT/mTOR pathway in pediatric acute B?cell lymphoblastic leukemia. Oncol Rep. 2019;41 (2):885-894.
[5] Malik B, McKerrow R, Harrington J, et al. ILC2 cells from severe allergic and eosinophilic asthma demonstrate increased expression of TSLP receptor (TSLPR) and enhanced proliferative capacity. Eur Respir J. 2021;58(suppl 65):PA823.
[6] Numazaki M, Abe M, Hanaoka K, et al. ASP7266, a Novel Antibody against Human Thymic Stromal Lymphopoietin Receptor for the Treatment of Allergic Diseases. J Pharmacol Exp Ther. 2022;380 (1):26-33.