ADAM9:超越蛋白水解的多功能調(diào)控因子
日期:2025-12-08 08:39:40
1. ADAM9結(jié)構(gòu)與生物學(xué)功能概覽
ADAM9是一種跨膜多結(jié)構(gòu)域蛋白,具有解整合素與金屬蛋白酶雙重功能,通過介導(dǎo)細(xì)胞黏附以及對(duì)底物蛋白進(jìn)行胞外域剪切來調(diào)控多種細(xì)胞表面蛋白的功能。ADAM9蛋白結(jié)構(gòu)由信號(hào)肽、前域、金屬蛋白酶域、整合素結(jié)合相關(guān)的解整合素域、富含半胱氨酸的結(jié)構(gòu)域、EGF樣結(jié)構(gòu)域、跨膜區(qū)及胞內(nèi)短尾部構(gòu)成。其中,前域負(fù)責(zé)維持酶的失活狀態(tài),通過去除前肽實(shí)現(xiàn)成熟酶的激活;金屬蛋白酶域則具備典型的催化活性,可剪切多種細(xì)胞膜蛋白;解整合素域參與介導(dǎo)細(xì)胞黏附;而胞內(nèi)區(qū)含信號(hào)轉(zhuǎn)導(dǎo)相關(guān)基序,使ADAM9 能整合外部刺激與胞內(nèi)反應(yīng)。ADAM9存在膜結(jié)合型與分泌型兩種主要同源異構(gòu)體,使其功能更加多樣化 [1]。
在生理過程中,ADAM9參與細(xì)胞黏附、遷移、蛋白質(zhì)剪切及組織重塑等關(guān)鍵事件,并在炎癥反應(yīng)、神經(jīng)系統(tǒng)發(fā)育及視網(wǎng)膜結(jié)構(gòu)維持中發(fā)揮作用。其金屬蛋白酶介導(dǎo)的外切作用可調(diào)控多種受體與黏附分子的剪切,包括 Tie-2、VEGFR2、VCAM-1等,從而影響血管生成、免疫細(xì)胞遷移與細(xì)胞間通訊。另一方面,ADAM9的表達(dá)變化與多種病理狀態(tài)密切相關(guān),如退行性疾病、組織損傷以及多種腫瘤。在癌癥中,ADAM9通過蛋白酶依賴與非依賴機(jī)制促進(jìn)腫瘤進(jìn)展、耐藥性及轉(zhuǎn)移,其高表達(dá)往往對(duì)應(yīng)更具侵襲性的臨床表現(xiàn)。總體而言,ADAM9兼具結(jié)構(gòu)多樣性與功能復(fù)雜性,是維持組織穩(wěn)態(tài)與驅(qū)動(dòng)疾病發(fā)生的重要分子,其分子特性為開發(fā)新型治療策略提供了關(guān)鍵靶點(diǎn)。
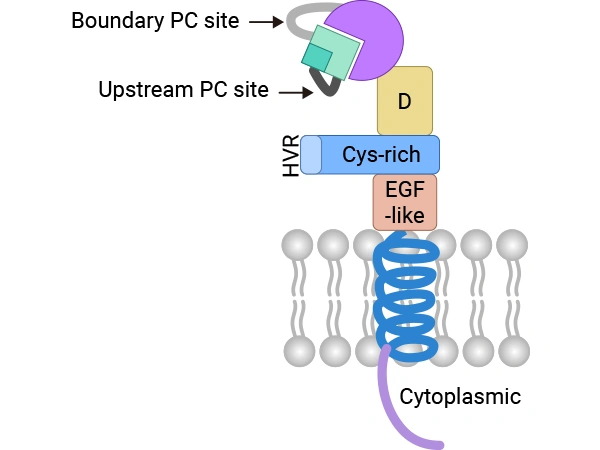
圖. ADAM9錨定在膜上時(shí)的C型結(jié)構(gòu)
來源:doi:10.3390/ijms21207790
2. ADAM9在疾病發(fā)展中的多重角色與機(jī)制
ADAM9作為一種多功能跨膜蛋白,不僅在腫瘤中有重要作用,也在多種免疫與炎癥性疾病中發(fā)揮關(guān)鍵調(diào)控作用,影響炎癥反應(yīng)、免疫細(xì)胞功能及疾病進(jìn)展。其獨(dú)特的結(jié)構(gòu)特征使其能夠參與復(fù)雜的信號(hào)網(wǎng)絡(luò)調(diào)控,通過酶活性和非酶活性兩種機(jī)制影響多個(gè)關(guān)鍵信號(hào)通路。
2.1 ADAM9在癌癥信號(hào)通路中的核心調(diào)控機(jī)制
在AKT信號(hào)通路調(diào)控中,ADAM9展現(xiàn)出精細(xì)的分子調(diào)控機(jī)制。其金屬蛋白酶結(jié)構(gòu)域能夠特異性識(shí)別并切割多種膜結(jié)合前體蛋白,包括生長(zhǎng)因子受體配體。例如,在口腔癌和乳腺癌研究中 [2][3],ADAM9通過調(diào)控HB-EGF的脫落過程,影響EGFR家族的活化狀態(tài),進(jìn)而激活下游PI3K/AKT信號(hào)軸。更重要的是,ADAM9還能通過其解整合素結(jié)構(gòu)域與整合素家族成員發(fā)生特異性相互作用,這種相互作用能夠改變整合素的構(gòu)象和功能狀態(tài),進(jìn)而影響FAK/Src信號(hào)復(fù)合物的組裝和活化 [4]。
在NF-κB通路調(diào)控方面,ADAM9表現(xiàn)出更為復(fù)雜的多層次控制能力。除了通過蛋白酶活性切割TNF家族前體蛋白外,ADAM9還能直接與IKK復(fù)合物中的重要調(diào)節(jié)亞基發(fā)生相互作用。這種直接相互作用可能影響IKK復(fù)合物的亞細(xì)胞定位和活化動(dòng)力學(xué) [3]。研究還發(fā)現(xiàn),ADAM9參與調(diào)控NF-κB與HIF-1α信號(hào)通路的交叉對(duì)話,這種交叉調(diào)控在腫瘤適應(yīng)缺氧微環(huán)境中發(fā)揮關(guān)鍵作用 [5]。
ADAM9在腫瘤血管生成中的調(diào)控作用表現(xiàn)出顯著的時(shí)空特異性。它不僅通過切割和釋放VEGF家族成員直接促進(jìn)血管生成,還能通過調(diào)控Angiopoietin-Tie2信號(hào)系統(tǒng)影響血管穩(wěn)定性 [3][4]。在胰腺癌研究中,ADAM9的表達(dá)水平與血管成熟度呈負(fù)相關(guān),提示其可能通過破壞血管正常化過程促進(jìn)腫瘤惡性進(jìn)展 [4]。
此外,ADAM9可通過影響多個(gè)關(guān)鍵信號(hào)節(jié)點(diǎn)協(xié)調(diào)上皮-間質(zhì)轉(zhuǎn)化(EMT)的調(diào)控過程 [6]。除了傳統(tǒng)的TGF-β和Wnt信號(hào)通路外,ADAM9還參與調(diào)控Hippo信號(hào)通路效應(yīng)分子YAP/TAZ的核質(zhì)穿梭。這種調(diào)控可能通過影響細(xì)胞機(jī)械感應(yīng)信號(hào)來實(shí)現(xiàn),因?yàn)锳DAM9與整合素的相互作用能夠改變細(xì)胞對(duì)細(xì)胞外基質(zhì)硬度的感知能力。
在治療抵抗機(jī)制方面,ADAM9通過建立復(fù)雜的反饋調(diào)控網(wǎng)絡(luò)影響腫瘤細(xì)胞的應(yīng)激反應(yīng) [3] [7]。在DNA損傷應(yīng)答中,ADAM9不僅影響ATM/ATR信號(hào)通路的活化,還能通過調(diào)控CHK1/2的磷酸化狀態(tài)影響細(xì)胞周期檢查點(diǎn)功能。在凋亡調(diào)控中,ADAM9通過影響B(tài)cl-2家族蛋白的磷酸化修飾和亞細(xì)胞定位,精細(xì)調(diào)節(jié)線粒體外膜通透性 [7]。
2.2 ADAM9在免疫細(xì)胞調(diào)控與炎癥反應(yīng)中發(fā)揮關(guān)鍵調(diào)控作用
ADAM9可通過與整合素(如αvβ3、α9β1)結(jié)合,激活PI3K/Akt和MAPK信號(hào)通路,促進(jìn)中性粒細(xì)胞的激活和趨化,增強(qiáng)其炎癥反應(yīng)能力。這一過程還涉及CXCR2信號(hào)的協(xié)同調(diào)控,提示ADAM9在炎癥相關(guān)疾病(如腫瘤微環(huán)境、慢性炎癥)中促進(jìn)免疫細(xì)胞遷移和激活 [8]。
ADAM9還可通過剪切多種膜結(jié)合蛋白(如MICA、TNF-α和IL-6R)破壞免疫監(jiān)視。例如,ADAM9介導(dǎo)MICA的脫落,產(chǎn)生可溶性MICA(sMICA),后者作為免疫誘餌抑制NK細(xì)胞介導(dǎo)的腫瘤細(xì)胞清除,從而促進(jìn)肝癌和結(jié)直腸癌等疾病的免疫逃逸 [9]。此外,ADAM9在慢性肝炎和非酒精性脂肪性肝炎(NASH)中通過調(diào)控IL-6等炎癥因子,加劇纖維化和癌變進(jìn)程。
3. ADAM9的藥物研發(fā)現(xiàn)狀
ADAM9是一種在生理和病理狀態(tài)下都具有多重功能的關(guān)鍵蛋白。特別是在癌癥領(lǐng)域,它通過蛋白酶依賴和非依賴的多種途徑驅(qū)動(dòng)腫瘤惡化,因此,ADAM9成為了藥物開發(fā)的一個(gè)潛在靶點(diǎn)。目前靶向ADAM9的在研藥物類型主要為ADC,適應(yīng)癥多為實(shí)體腫瘤。以下是ADAM9在研ADC管線:
| 藥物 | 藥物類型 | 適應(yīng)癥 | 在研機(jī)構(gòu) | 最高研發(fā)階段 |
|---|---|---|---|---|
| AEX-6003 | ADC | 腫瘤 | ImmunoGen | 臨床前 |
| DB1317 | ADC | 晚期惡性實(shí)體瘤,去勢(shì)抵抗性前列腺癌 | 映恩生物制藥(蘇州) | 臨床1期 |
| MGC-028 | ADC | 晚期惡性實(shí)體瘤,大腸腺癌、膽管癌、結(jié)直腸癌、非小細(xì)胞癌等 | MacroGenics | 臨床1期 |
| IMGC-936 | ADC | 晚期惡性實(shí)體瘤 | MacroGenics, ImmunoGen | 臨床1/2期 |
(數(shù)據(jù)來源于Pharmsnap)
4. 相關(guān)產(chǎn)品推薦
● ADAM9重組蛋白
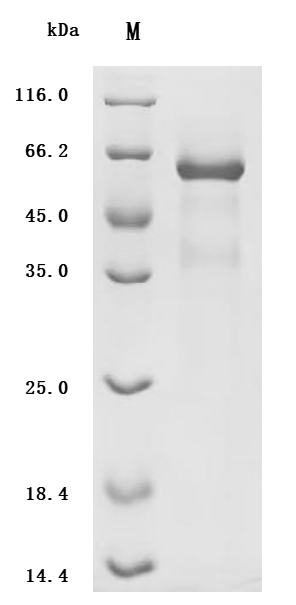
(Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
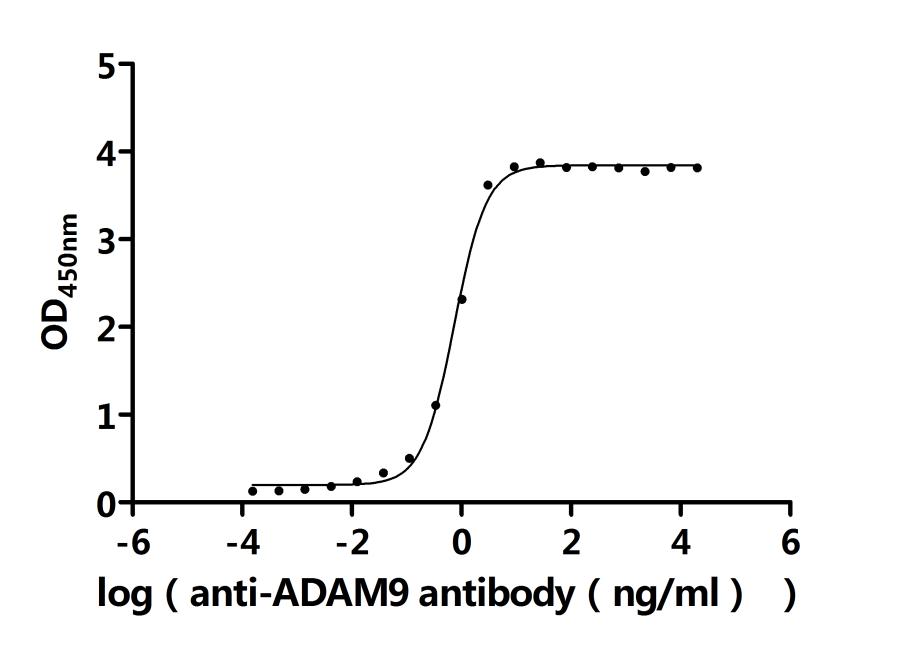
Activity: Measured by its binding ability in a functional ELISA. Immobilized Human ADAM9 at 2μg/ml can bind Anti-ADAM9 recombinant antibody (CSB-RA618774MA1HU). The EC50 is 0.9401-1.088 ng/mL.
Recombinant Macaca fascicularis ADAM9 metallopeptidase domain 9 (ADAM9), Partial,
(CSB-MP7133MOVd7)

(Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
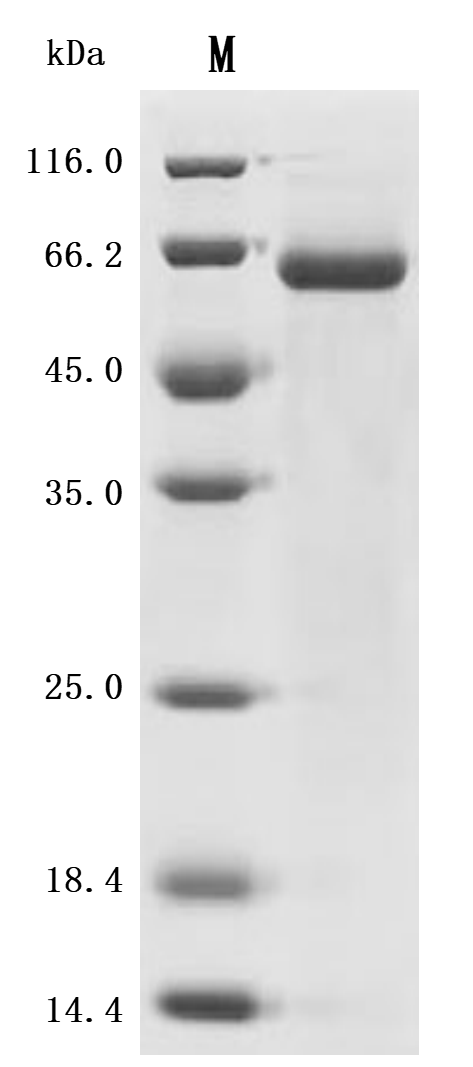
(Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
● ADAM9抗體
ADAM9 Antibody (CSB-PA618774ESR1HU)
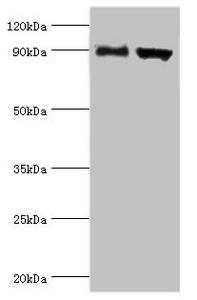
Western blot
All lanes: Disintegrin and metalloproteinase domain-containing protein 9 antibody at 2μg/ml
Lane 1: Mouse liver tissue
Lane 2: Mouse heart tissue
Secondary
Goat polyclonal to rabbit IgG at 1/10000 dilution
Predicted band size: 91,73 kDa
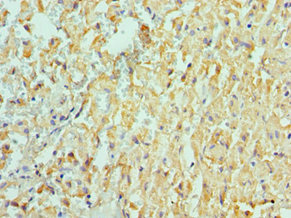
Immunohistochemistry of paraffin-embedded human liver cancer using CSB-PA618774ESR1HU at dilution of 1:100
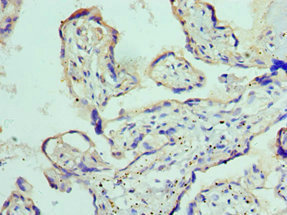
Immunohistochemistry of paraffin-embedded human placenta tissue using CSB-PA618774ESR1HU at dilution of 1:100
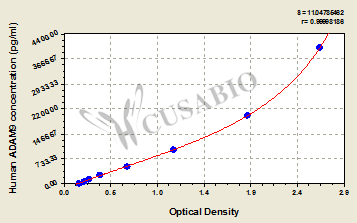
● ADAM9 ELISA試劑盒
參考文獻(xiàn):
[1] Chou, C. W., Huang, Y. K., Kuo, T. T., Liu, J. P., & Sher, Y. P. (2020). An Overview of ADAM9: Structure, Activation, and Regulation in Human Diseases. International journal of molecular sciences, 21(20), 7790.
[2] Buranaphatthana, W., Wu, S., Makeudom, A., Sastraruji, T., Supanchart, C., & Krisanaprakornkit, S. (2021). Involvement of the A disintegrin and metalloproteinase 9 in oral cancer cell invasion.. European journal of oral sciences, e12775 .
[3] Zhou, R., Cho, W., , V., Cheuk, W., So, Y., Wong, S., Zhang, M., Li, C., Sun, Y., Zhang, H., Chan, L., & Tian, M. (2020). ADAM9 Mediates Triple-Negative Breast Cancer Progression via AKT/NF-κB Pathway. Frontiers in Medicine, 7.
[4] Oria, V., Lopatta, P., Schmitz, T., Preca, B., Nystr?m, A., Conrad, C., Bartsch, J., Kulemann, B., Hoeppner, J., Maurer, J., Bronsert, P., & Schilling, O. (2019). ADAM9 contributes to vascular invasion in pancreatic ductal adenocarcinoma. Molecular Oncology, 13, 456 - 479.
[5] Zhu, L., Zhao, Y., Yu, L., He, X., Wang, Y., Jiang, P., Yu, R., Li, W., Dong, B., Wang, X., & Dong, Y. (2021). Overexpression of ADAM9 decreases radiosensitivity of hepatocellular carcinoma cell by activating autophagy. Bioengineered, 12, 5516 - 5528.
[6] Moriwaki, M., Le, T., Sung, S., Jotatsu, Y., Yang, Y., Hirata, Y., Ishii, A., Chiang, Y., Chen, K., Shigemura, K., & Fujisawa, M. (2022). Relevance of A Disintegrin and Metalloproteinase Domain-Containing (ADAM)9 Protein Expression to Bladder Cancer Malignancy. Biomolecules, 12.
[7] Ueno, M., Shiomi, T., Mochizuki, S., Chijiiwa, M., Shimoda, M., Kanai, Y., Kataoka, F., Hirasawa, A., Susumu, N., Aoki, D., & Okada, Y. (2018). ADAM9 is over‐expressed in human ovarian clear cell carcinomas and suppresses cisplatin‐induced cell death. Cancer Science, 109, 471 - 482.
[8] Amêndola, R., Martin, A., Selistre-De-Araújo, H., Paula-Neto, H., Saldanha-Gama, R., & Barja-Fidalgo, C. (2015). ADAM9 disintegrin domain activates human neutrophils through an autocrine circuit involving integrins and CXCR2. Journal of Leukocyte Biology, 97.
[9] Arai, J., Otoyama, Y., Nozawa, H., Kato, N., & Yoshida, H. (2022). The immunological role of ADAMs in the field of gastroenterological chronic inflammatory diseases and cancers: a review. Oncogene, 42, 549 - 558.